
免疫分析法是使用抗体检测不同物质的实验分析方法。它们通常用于生命科学行业的生物分析和生化实验室。这些方法包括酶联免疫吸附试验(ELISA)、酶免疫分析(EIA)、免疫印迹 (WB)、放射免疫分析(RIA)、蛋白质阵列、免疫组化(IHC)或免疫聚合酶链反应(Immuno-PCR)。在各种免疫分析法中,待测物的检测都可能受到干扰的影响。如经常发生的交叉反应、非特异性结合和基质效应。干扰物质在真实标本中以或多或少的显著浓度水平存在,并与待测物或捕获检测抗体相互作用。通过使用一种新的缓冲液(Lowcross-Buffer),替代传统缓冲液,大多数干扰影响都可以避免。通过这种替换,提高了分析方法的质量和分析方法开发的效率。
尼尔斯·杰尼因其在免疫系统的构建和控制特异性方面的贡献获得1984年诺贝尔医学奖,他在颁奖演讲中提到,每一种抗体都是多特异性的。他将这一说法与免疫反应早期阶段的抗体产生联系起来。与目标分析物具有高亲和力的抗体偶尔会显示出令人惊讶的结果:在包被捕获抗体的免疫检测中,免疫印迹膜中不必要的条带被染色,蛋白质阵列上得到错误斑点的荧光信号以及空白样本的高背景信号。ELISA检测中,得到阴性信号的高背景或假阴性结果。由于干扰效应造成的错误结果可能导致后续成本浪费和错误诊断。
所有的免疫分析方法的特征是在目标分析物和抗体之间的结合反应。这些方法存在的问题是经常发生的干扰,导致了错误的检测,这个问题至今未得到充分地解决。典型的干扰有非特异性结合,导致较差的信噪比和高背景, 交叉反应和基质效应。简单地说,这些效应大多是基于分析物、捕获抗体或检测抗体与外部物质或表面的直接相互作用。图1表示了一种典型干扰效应的简化方案。在技术文献中经常被描述的已知的干扰因素有如异嗜性抗体和HAMAs(人抗小鼠抗体)、类风湿性因子、白蛋白、补体,溶菌酶以及其他等。
免疫分析标记带来的干扰
在免疫分析中标记检测抗体非常常见,譬如在竞争法中,标记待测分析物。经常使用的标记有酶(碱性磷酸酶或(辣根)过氧化物酶)、荧光染料、放射性同位素或DNA(用于免疫PCR)。不必要的影响也出现在这里。危险在于,使用荧光染料作为标记,这类疏水染料会改变检测抗体的结合能力,导致染料本身的非期望的结合,且降低了标记 蛋白的溶解度。此外,抗原与抗体的结合也会变弱。例如,这些非特异性效应会导致抗体与表面(图1A和B)、与样品中的外部蛋白质(图1C)或对捕获抗体(图1D)的结合增加。在这些情况下,会导致在没有分析物存在时出现假阳性或整个检测出现高背景。在蛋白质芯片上观察到单个斑点的背景荧光增加,或信噪比完全变糟糕。同样,血清样本中的蛋白质或抗体也可以与荧光染料结合,减少甚至封闭染料的荧光。因此,一些研究人员已经建议放弃荧光染料作为蛋白质阵列的标记或选择其他标记。蛋白质芯片上的反应是非常复杂的,因为在一个反应体系中同时使用多种不同的捕获抗体和标记的检测抗体。因此,样本中蛋白质或标记抗体与单点的非特异性结合的概率升高, 同时样本中成分与抗体的结合带来的干扰效应也随之增加。
交叉反应带来的干扰
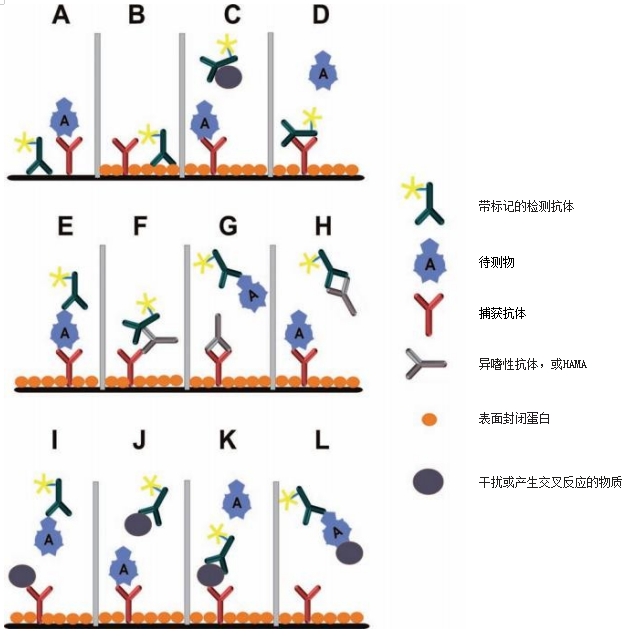
图1: 在免疫分析中可能出现的不同干扰效应的示意图。
A: 标记的检测抗体与未封闭的表面的非特异性结合。结果是假阳性信号。
B: 标记的检测抗体与封闭表面的非特异性结合。尽管表面被封闭,但抗体与封闭蛋白相结合。结果是假阳性信号。
C: 干扰蛋白与检测抗体的Fc片段结合,并在空间上阻碍待测物的结合。结果是假阴性信号。
D: 捕获抗体与检测抗体的Fc片段结合。结果是假阳性信号。待检测物不能再与捕获抗体结合。
E: 不受影响的试验,没有任何干扰。理想的状态。
F: 通过异嗜性抗体或HAMAs进行的桥接结合。通过此方法,捕获抗体与检测抗体连接,从而产生假阳性信号。
G: 一种与捕获抗体具有抗独特型结合特性的HAMA。干扰抗体结合在捕获抗体Fab片段的高度可变区域,从而阻止了待测物的结合。因此,就会出现假阴性信号。
H:一种与检测抗体具有抗独特型结合特性的HAMA。干扰抗体结合在检测抗体Fab片段的高度可变区域,并阻止待测物的结合。结果,出现了假阴性信号。
I:干扰物质与捕获抗体的交叉反应性。结果是假阴性信号。
J:干扰物质与检测抗体的交叉反应性。结果是假阴性信号。
K:与捕获抗体和与检测抗体的交叉反应性。这种现象在实践中很少出现,这种抗体的特异性肯定较低。这种干扰现象也可以发生在待测物具有蛋白质保守氨基酸序列,该序列也出现在其他蛋白质上。
L:样本中的其他蛋白质掩蔽待测物,使其表位被封闭,无法与捕获抗体结合,或空间位阻情况严重。结果是假阴性信号。
非特异性结合带来的干扰
与交叉反应密切相关的是非特异性结合。然而,两者在分子水平上的机理有所不同。在日常的实验室工作中, 这些差异不明显。交叉反应中,造成交叉反应的物质是已知的,并且它的交叉反应性可以定量,譬如与交叉反应物的浓度竞争关系。而在非特异性结合的情况下,结合涉及的物质, 远远超过目标分析物(如与白蛋白或免疫球蛋白的非特异性结合)或与表面(如ELISA孔或免疫印迹膜表面)或蛋白质芯片中的固定抗体斑点。
基质效应
基质效应是样本中所含成分带来的干扰效应的总和,影响目标分析物的检测。如果产生干扰的真正分子原因还没有确定,但人们知道它来自于样本,那么一般就称之为“基质效应”。从一种效应到另一种效应的边界是不固定的,有时并不清晰。一些基质效应来自“抗动物抗体”,另一些来自异嗜性抗体,或来自内源性干扰,或仅仅来自粘度、ph值或仅仅来自盐浓度。
抗动物抗体产生的干扰
人抗动物抗体(HAAA)可为IgG-、IgA、IgM或IgE型。它们是免疫系统应答的一部分,与动物来源的免疫球蛋白结合。HAAAs在许多诊断性免疫分析中是众所周知的干扰物,有时可能是80%的临床标本的一部分——取决于具体应用研究。HAAAs的浓度最高可达每毫升数毫克。
HAMAs不仅来源于抗体治疗,长期接触家畜和宠物,最终也会形成针对这些动物的抗体。有人在患者的血清中发现了针对兔子、老鼠、狗、仓鼠的抗体。这些抗动物抗体干扰了一些具有不同亲和力和不同问题的检测抗体。一些干扰抗体不仅针对检测抗体的Fc片段,也针对检测抗体的Fab片段。这可能导致正确结合减少或完全阻碍,从而导致假阴性信号(图1G和H)。如果HAAAs与Fc片段结合,它们被称为抗同型干扰。如果它们结合到高度可变的Fab片段上,它们就被称为抗独特型干扰。
异嗜性抗体带来的干扰
泰伯医学词典将异嗜性抗体定义为“与特定抗原以外的其他抗原结合的抗体”。异型抗体可为IgG、IgA、IgM或IgE型。特别是IgM型在风湿病患者的血清中起着特殊的作用。这些血清中含有高浓度的所谓类风湿性因子。类风湿性因子是IgM抗体,可与人类抗体的Fc部分结合,因此也与实验中使用的抗体的Fc部分结合,且与物种无关。因此,风湿病血清将捕获与检测抗体连接起来,导致假阳性结果。这同时也是异嗜性抗体的一般干扰机制。风湿病血清的效应类似于HAAAs的效应。与HAAAs相比的区别在于异嗜性抗体的来源,他们不是建立在与动物免疫球蛋白反应的基础上,而是早期免疫应答的多特异性抗体或来源不明的干扰性抗体。
因HAAAs或异嗜性抗体造成的干扰被发现已有30多年。干扰抗体是来自动物源的一般弱结合抗体,主要干扰由于分析物浓度低,血清或血浆样本需低稀释度稀释的分析。向样本缓冲液中添加阻断物——通常是非特异性血清、抗体片段或高浓度的动物免疫球蛋白——能够通过竞争减少HAAAs或异嗜性抗体的干扰效应,但不能完全避免。
样品内源性物质带来的干扰
即使是标本中天然存在的蛋白质也会干扰免疫分析。人血清中众所周知的干扰物质有白蛋白、补体、溶菌酶和纤维蛋白原。低分子量的分析物可以与白蛋白结合,这使得抗体与分析物的结合变得困难。许多激素都与转运蛋 白结合,这也可能为免疫分析带来困难。此外,许多蛋白质具有结合其他物质和蛋白质的能力。这种结合能力通常是各自蛋白质生物学功能的重要组成部分。白蛋白、补体和C反应蛋白(CRP) 是多种物质的天然受体。因此,非特异性结合甚至交叉反应——如与抗体的反应一样——都是可能发生的。这使得在免疫检测中识别某些分析物变得复杂。内源性 蛋白可以作为一种干扰因子与抗体结合(图1C,I-K)或掩蔽目标分析物(图1L)。例如,溶菌酶能非特异性地与具有低等电点的蛋白质结合。因此,低等电点(约5)的抗体可以与之结合,并在捕获抗体和检测抗体之间建立桥梁。需要提到的一个重要方面是,含有大量脂质的标本的干扰,因为一些分析物是脂溶性的,且抗体与分析物之间的结合可能也会受到脂质的影响。
钩状效应
钩状效会导致假阴性结果,但与其他干扰效应不同的是,它不是通过与干扰因素的相互作用而产生。
免疫分析时,当样本与分析抗体直接混合,且分析物的浓度非常高时,钩状效应就有可能发生。在这种情况下,当分析物的高浓度超过分析抗体的浓度时, 捕获抗体和检测抗体会出现饱和。因此高浓度被判读为远低于实际的低浓度, 从而导致对真实浓度的显著低估。在实践中,通过使用更高浓度的检测抗体或者稀释样本,可以避免钩状效应。或者,必须对实验进行系统化稀释,以确保检测值不受钩状效应的影响。已知的可能受到钩状效应影响的临床参数有: CRP、AFP、CA125、PSA、铁蛋白、催乳素及TSH等。
使用LowCross Buffer®防止干扰
造成所描述的干扰效应的原因是相似的。干扰因子与抗体或分析物之间存在不必要的从低到中的亲和作用。标记抗体与其他蛋白质或表面的低亲和力结合或中亲和力结合,同样抗体与结构相关物质低到中亲和交叉反应。LowCross Buffer®利用了这些干扰效应的共同之处:干扰反应弱于真实分析物的特异性结合。当然,很少有因发生非常高的亲和的交叉反应,达到与真正特定性结合相同的结果。在这种情况下, 人们必须谈论一个特定的结合,并且在原则上有一个针对两种不同物质的抗体。因此,这种抗体根本不能用于特定的分析。Low Cross Buffer® 是专门开发来消除低和中亲和力结合,但不会对高特异性的高亲和力结合产生任何负面影响。
图2到图5显示使用LowCross Buffer®可防止免疫分析中典型的干扰效应的不同示例。图2显示了在蛋白芯片应用中使用LowCross Buffer®可降低高背景,并将信噪比从3.4提高到17.3。在这个实验中,对不同多克隆抗EPIL抗体(EPIL=早期胎盘胰岛素样生长因子) 的适用性进行了测试。抗体使用浓度为500µg/ml、体积为1.8 nl/spot通过生物芯片打点机(GMS 417)固定在氨基硅烷化的微阵列载玻片上。随后,将2ml的EPIL过度表达细胞系(SKBR3) 培养基与染料Oyster650P混合,此时培养基内蛋白质被标记。分别使用LowCross Buffer®和PBS按照1:20稀释培养基,加在载玻片上进行孵育。冲洗载玻片后,用荧光扫描仪(GMS 418) 进行读取,并用ImaGene分析数据。通过使用LowCross Buffer®可以明显降低背景信号,从而使得更好地区分单个抗体是否适用于检测EPIL。
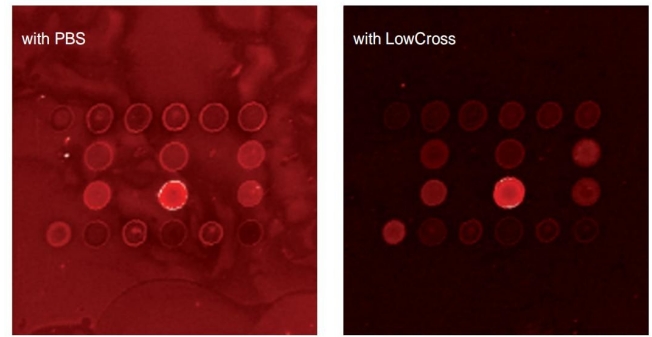
图2: 减少检测抗体与蛋白质芯片表面的非特异性结合。通过使用LowCross-Buffer®,将信噪比从3.4提高到17.3。(数据源自N. Dankbar, university of Münster)
图3显示用westen blotting法检测来自肝细胞和HeLa细胞的角蛋白4、5 和6,其中通过交叉反应非特异性结合检测到比正确条带更多的条带。蛋白质样品在12.5% SDS-聚丙烯酰胺凝胶上电泳跑样,然后印迹到硝基纤维素膜上。蛋白质样本中的细胞角蛋白的westen blotting检测方法采用改进的标准流程。抗细胞角蛋白抗体用LowCross Buffer® 或 TTBS(Tween- Tris缓冲盐水)按照1:2500比例稀释,用碱性磷酸酶标记的二抗进行检测(二抗用LowCross缓冲液®或TTBS 按照1:1250比例进行稀释),再加入底物BCIP/NBT显色。如果没有LowCross Buffer®的帮助, 很难揭示非特异性结合反应的确切分子原因。由于其他细胞角蛋白及其裂解产物或与肝脏或HeLa细胞的细胞破裂产生的不同蛋白质的非特异性结合,可能导致交叉反应发生。用LowCross buffer®替换TTBS,稀释一抗和二抗,可以将非必要的结合减少,细胞角蛋白只在56 -60kDa的正确分子量区域内被染色。
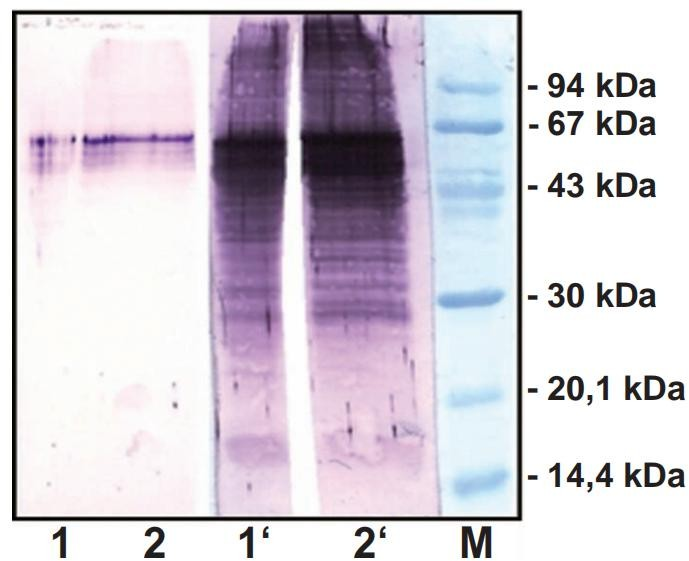
图3: Western blotting法检测细胞角蛋白4、5和6。图中显示了实验中使用LowCross Buffer®和TTBS检测的效果对比。LowCross Buffer® 可以完全防止不必要的结合。细胞角蛋白4、5和6在56-60kDa之间,使用LowCross Buffer® 可清晰地被检测到。泳道1和1'样本来自肝细胞,泳道2和2'样本来自Hela细胞。M为分子量marker,用酰胺黑染色。印迹膜是硝酸纤维素膜porablot NCP。
图4 显示了基质效应如何影响ELISA。通过这种模型分析(由Candor Bioscience公司开发),系统地诱导了基质效应。用兔血清作为基质,加入一定浓度的C反应蛋白。使用捕获抗体(clone C2,1 µg/ml))和生物素化检测抗体(clone C6, 2 µg/ml)。加入的血清样品分别用PBS-BSA缓冲液或LowCross-Buffer®按照1:2进行稀释,用ELISA检测。通过加入辣根过氧化物酶结合物及TMB底物进行检测。
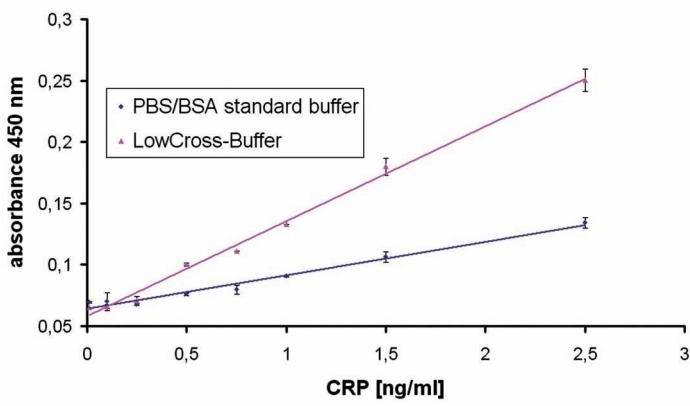
图4:ELISA法检测家兔血清中的CRP。 LowCross-Buffer®通过去除基质效应来提高灵敏度。
基质效应的确切分子基质未知,它会导致校准曲线的灵敏度变差。CRP蛋白由于其生理特征,能够结合许多蛋白质和其他物质,可能显著降低表位的可用性。虽然不能排除图1(I-L)中所示的干扰效应发生的可能,但大概率会发生图1(L)所示的干扰效应。LowCross Buffer®可防止CRP与兔血清内源性物质结合,从而将校准曲线的灵敏度提高3倍。
图5是用于豚鼠免疫毒理学研究的抗豚鼠免疫球蛋白的ELISA示例。在本试验中,特异性对照(A1-A12行)和空白值(H1-H12)的假阳性结合破坏了数据评估。LowCross Buffer®的使用防止了假阳性信号,而且使B至G行1-6或B至G行7-12的浓度检测成为可能。使用山羊抗豚鼠IgG F(ab')2作为捕获抗体,并使用生物素化的山羊抗豚鼠IgG(Fcγ)作为检测抗体。豚鼠IgG用LowCross Buffer®或PBS进行稀释。PBS-BSA缓冲液用作封闭缓冲液。用链霉亲和素过氧化物酶和邻苯二胺进行检测。
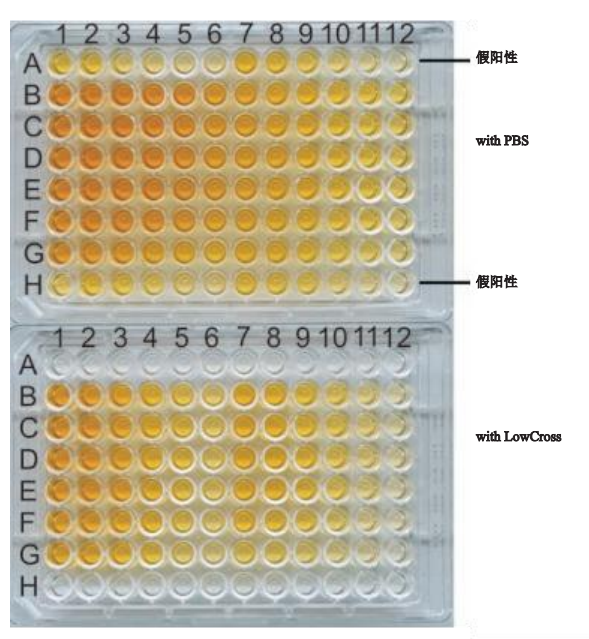
图5: 在用豚鼠IgG进行ELISA实验中,通过使用LowCross-Buffer®防止假阳性结合(A1- 12行为对照组,H1-12为空白组)。
结论
免疫分析中用于生物分析和诊断目的的抗体的使用,同时伴随着干扰现象的产生。在过去30年赵成成干扰的多种分子机制被发现,人们对其进行评估,从而制定预防策略。在当今的技术发展水平上,许多干扰影响都可以最小化,而LowCross Buffer®对此做出了重要贡献。LowCross Buffer®可使不同分子原理的不同干扰效应最小化,适用于不同的免疫分析。此外,LowCross Buffer® 还可以防止HAMAs和类风湿性因子的干扰效应、免疫组织化学应用中的非特异性结合以及免疫PCR中的假阳性条带。总之,优化实验所需的时间和成本可以大大减少和简化,同时提高可靠性。
相关产品推荐
Candor Bioscience 100500 LowCross Buffer
Candor Bioscience 180500 Assay defender
文献引用
[1] Jerne, N.K., Science 229 (1985), 1057-1059
[2] Kaplan, I.V., Levinson, S.S., Clinical Chemistry 45:5 (1999), 616-618
[3] Miller, J.J., Clinical Laboratory International 28, 2 (2004), 14-17
[4] Selby, C., Ann Clin Biochem 36 (1999), 704-721
[5] Patton, W.F., Electrophoresis 21 (2000), 1123-1144
[6] MacBeath, G., Nat. Genet. 32 (2002), 526-532
[7] Kusnezow, W., Hoheisel, J.D., J. Mol. Recognit. 16 (2003), 165-176
[8] Miller, J.J., Valdes, R.Jr., J Clin Immunoassays 15 (1992), 97-107
[9] Wood, W.G., Scand. J. Clin. Lab. Invest. Suppl. 205 (1991), 105-112
[10] Kricka, L.J., Clinical Chemistry 45:7 (1999), 942-956
[12] Span, P.N., Grebenchtchikov N., Geurts-Moespot, J., Sweep, C.G.J., Clinical Chemistry 49:10 (2003), 1708-1709
[13] Gallagher, S., Immunoblot Detection, in: Current Protocols in Protein Science, John E. C. et al., eds., 1995, John Wiley & Sons
